
Le projet COVID-PHYM auquel vous avez participé avec la Fondation Ibercivis et le Groupe Biophym de l'Institut pour la Structure de la Matière de la SCCI présente ses premiers résultats sous la forme d'une prépublication et en l'absence d'un examen par les pairs. L'équipe scientifique travaille toujours sur le projet pour pouvoir donner des résultats concluants.
Le projet visait à réaliser des simulations de l'interaction des médicaments utilisés contre le virus Ebola, l'infection par le VIH, la grippe ou l'hépatite B avec les mécanismes de réplication du génome du virus du SRAS-Co-V, dans le but de disposer de médicaments efficaces contre le coronavirus est essentiel pour réduire la gravité et la mortalité de la maladie.
Dans le développement de ce projet, la participation des citoyens par le biais du réseau de calcul distribué Boinc, que nous dirigeons depuis la Fondation Ibercivis, a joué un rôle fondamental. Des milliers d'ordinateurs à travers le monde ont été connectés à un grand réseau pendant les mois d'avril à juin 2020 pour apporter leur capacité de traitement aux calculs nécessaires à la réalisation de l'expérience. À vous tous, en tant que participants individuels, et à la communauté Boinc
Merci beaucoup !
Ensemble de ténofovir et de remdesivir avec la polymérase SARS-CoV-2 et l'ARN naissant de la matrice
Résumé
Le repositionnement du remdesivir et du ténofovir contre la COVID-19 n'a montré que des preuves partielles d'amélioration des résultats cliniques, respectivement dans les essais cliniques et les études observationnelles. La justification de cette efficacité incohérente reste inconnue. Ici, nous avons développé une approche d'amarrage d'ensemble pour les formes triphosphatées actives des deux antiviraux avec la polymérase SARS-CoV-2 et le complexe de la chaîne ARN, sous l'hypothèse que l'observation clinique pourrait s'appuyer sur les spécificités de l'interaction médicament-cible. Notre cadre de modèle a permis une reconstruction précise de l'ensemble remdesivir, qui présentait la plus forte affinité de liaison et une stabilité de pose proche de son homologue naturel dATP. Nous avons en outre observé un ensemble de caractéristiques du complexe de ténofovir qui suggère une interaction fonctionnelle mais sous-optimale, résultant probablement en une inhibition virale limitée en l'absence de concentration intracellulaire élevée dans les tissus cibles. Nos résultats justifient l'efficacité mixte des composés à base de ténofovir contre le SRAS-CoV-2 et soulignent la pertinence de la disponibilité intracellulaire des analogues nucléotidiques par rapport au tropisme viral.
Introduction
Les thérapies définitives pour prévenir et traiter la COVID-19, la maladie causée par le SRAS-CoV-2, font toujours défaut. Le déploiement mondial de vaccins potentiellement efficaces prendra probablement plusieurs mois, voire des années. Parallèlement, il existe un besoin urgent d'alternatives qui contribuent à réduire la mortalité et à protéger les plus vulnérables. Le repositionnement (trouver une nouvelle utilisation thérapeutique pour un médicament déjà connu ) est l'option la plus rapide pour administrer un traitement car l'innocuité et la tolérance ont déjà été vérifiées; Cependant, il est difficile de décider quels médicaments doivent être priorisés, tout comme la détermination des meilleures approches précliniques à développer avant que l'évaluation clinique ne soit atteinte.
À ce jour, seuls deux antiviraux repositionnés ont montré des preuves partielles dans la prévention de la morbidité COVID-19: le remdesivir comme traitement des patients COVID-19 sévères dans un essai clinique randomisé et le ténofovir (comme promédicament ténofovir disoproxil fumarate, TDF) dans une rétrospective étude observationnelle suivant des individus séropositifs sous antiviraux. Le remdesivir et le ténofovir ont été initialement conçus pour inhiber la polymérisation de l'ATP dans la chaîne d'acides nucléiques en croissance dans la polymérase du virus Ebola et la transcriptase inverse du VIH, respectivement.
Un récent essai clinique randomisé aux États-Unis a rapporté une récupération plus courte pour les patients hospitalisés par COVID-19 traités par remdesivir par rapport au placebo, mais l'étude n'a pas montré de diminution significative de la mortalité. Cependant, un essai antérieur en Chine n'a rapporté aucune différence dans les résultats cliniques pour le traitement par remdesivir par rapport au placebo, bien que cet essai ait eu une puissance statistique insuffisante en raison de ne pas atteindre la taille d'échantillon prévue. D'autre part, des preuves de l'efficacité prophylactique pré-exposition du ténofovir analogue nucléotidique, en particulier du TDF en association avec l'émcitribacine (FTC), ont été suggérées dans une étude observationnelle récente évaluant les résultats de l'infection par le SRAS-CoV-2 chez les patients VIH sous traitement antirétroviral en Espagne. Les personnes prenant du TDF / FTC pour leur infection par le VIH présentaient un risque significativement plus faible d'infection par le SRAS-CoV-2 et d'hospitalisation par rapport aux personnes prenant d'autres antiviraux ou prenant le promédicament à base de ténofovir alafénamide fumarate (TAF) avec FTC. Une tendance protectrice similaire pour le TDF / FTC sur la mortalité par COVID-19 a été observée en Afrique du Sud par rapport aux régimes à base de zidovudine ou d'abacavir. Néanmoins, les résultats doivent encore être confirmés par des essais cliniques randomisés. Cet écart entre les différentes promédicaments du ténofovir conduisant à une efficacité mixte est inexpliqué, au-delà de l'existence potentielle de facteurs de confusion dans l'analyse, qui a été en partie exclue pour la cohorte espagnole.
Afin d'obtenir une inhibition virale, un acide nucléique analogue doit se lier à la polymérase virale à l'intérieur des cellules infectées après métabolisation en leurs formes actives. En particulier, pour que le ténofovir et le remdesivir bloquent la réplication du SRAS-CoV-2, il est nécessaire que leurs formes triphosphate actives soient capables de se lier fortement à l'ARN polymérase virale en présence d'ARN naissant, en remplaçant leur homologue naturel, la désoxyadénosine triphosphate dATP, qui en son tour conduit à l'incorporation de l'antimétabolite dans la chaîne et à l'arrêt de la polymérisation. Ainsi, l'affinité et la stabilité des antiviraux dans la poche active de la polymérase virale définissent toute autre inhibition.
Ici, nous avons conçu une approche d'amarrage d'ensemble dérivée de structures cristallines et mise en œuvre avec un échantillonnage étendu utilisant un calcul distribué par des volontaires, pour prédire l'emplacement de liaison, l'affinité et la stabilité des formes actives remdesivir-triphosphate, ténofovir-diphosphate et dATP avec le SARS-CoV -2 ARN polymérase ARN-dépendante (RdRp-CoV2) et le complexe matrice-chaîne ARN naissante, et pour déterminer les limitations potentielles découlant de leurs structures moléculaires.
Résultats
Nous avons effectué des simulations d'amarrage d'ensemble en utilisant la structure de microscopie cryo-électronique de la nsp12 dans un complexe avec un ARN modèle naissant et chacun des éléments suivants: remdesivir-triphosphate, ténofovir-diphosphate et dATP.
Les énergies de liaison relatives calculées ( liaison ΔG ) ont montré que le remdesivir présentait la liaison la plus forte (plage de précision -8,7 à -8,5 kcal / mol), suivi du dATP (-8,6 à -8,4 kcal / mol) et du ténofovir (-7,7 à -7,5 kcal) / mol). Les trois ligands partageaient le même site de liaison et ont été forcés d'adopter une conformation différente afin de permettre l'insertion du nucléotide entrant dans l'ARN naissant. Les structures d'ancrage des ensembles dATP, remdesivir et ténofovir sont présentées dans la figure 1. L'inclusion des chaînes ARN / ions magnésium dans l'analyse a réduit la liaison ΔG calculéepour les trois ligands tout en conservant un gradient d'affinité similaire (voir matériel supplémentaire, S2). Nous avons en outre observé que les principaux sites de liaison des ligands étaient situés dans une poche différente de celle des sites de liaison de l'ensemble sans matrice-ARN naissant (RdRp-CoV2-NoRNA).
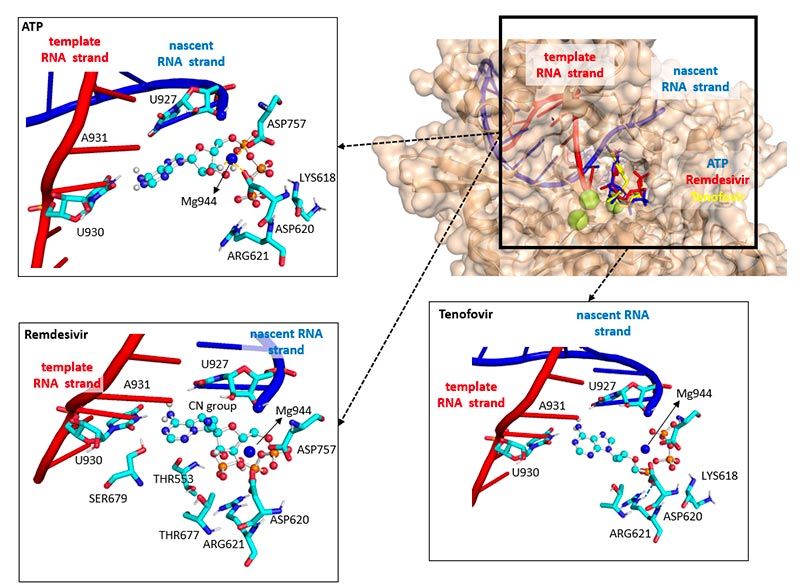
Figure 1: Les ligands sont affichés sous forme de balle et de bâton; Les résidus d'ARN et d'acides aminés interagissant avec les ligands sont représentés sous forme de bâtonnets; et les ions magnésium sont représentés par une sphère bleue de Van der Waals. Le carré représente la grille approximative utilisée pour effectuer les études d'amarrage. L'analyse des interactions a été réalisée à l'aide du profileur d'interaction Protein-Ligand (PLIP) [41] et Discovery Studio. Les images ont été préparées en utilisant Pymol 2.4.0.
Nous avons observé que les conformations d'énergie de liaison les plus faibles ne montraient pas toujours les interactions attendues entre les brins d'ARN matriciels naissants et le ligand analysé. Ainsi, nous avons recherché les poses avec une interaction maximale avec le brin d'ARN matrice et calculé la liaison ΔG . Dans le cas de l'ATP et du remdesivir, nous avons constaté que ces poses restent proches de la liaison ΔG calculée la plus basse (environ 0,1 kcal / mol), tandis que l'ensemble de ténofovir a montré une plus grande différence entre la pose avec les interactions ARN et les poses de liaison ΔG les plus basses. (environ 0,5 kcal / mol). Le facteur le plus probable de la liaison ΔG inférieure du remdesivir par rapport à l'ATP est la liaison H supplémentaire entre le groupe cyano et le nucléotide U927 du brin d'ARN naissant.
Pour les trois ligands, l'ion Mg2 + et l'ARG621 chargé ont contribué à stabiliser la position du groupement triphosphate par des interactions électrostatiques et sel-pont. En outre, des liaisons H typiques entre le nucléotide uracile du brin d'ARN matrice (U930) et (comme) les anneaux d'adénosine présentés dans les trois ligands ont été observées soutenant la formation d'un complexe de liaison entre le ligand entrant et le brin d'ARN matrice, avant le insertion dans le brin d'ARN naissant. De plus, les interactions hydrophobes entre les U927 et A931 dans la matrice et les brins d'ARN naissants ont aidé à mieux stabiliser les ensembles dATP et remdesivir. Cependant, pour le ténofovir, les interactions observées avec les nucléotides dans l'ARN naissant étaient différentes. En particulier, une liaison H s'est formée entre le cycle adénine du ténofovir et le nucléotide U927. Cette disposition a empêché la formation des interactions hydrophobes observées dans les ensembles dATP et remdesivir. Fait intéressant, une pose d'énergie de liaison la plus faible loin du site central d'inhibition a été trouvée pour le ténofovir, mais pas pour le remdesivir ni le dATP (voir la figure S2), ce qui suggère un site compétitif non fonctionnel pour le ténofovir.
En résumé, l'amarrage moléculaire de l'ensemble a été réalisé en utilisant le dATP, le remdesivir-triphosphate et le ténofovir-diphosphate liant le récepteur cible RdRp-CoV2 avec l'ARN de matrice naissant. L'ensemble du remdesivir a été reconstruit avec précision, par rapport aux modèles précédents, et la forme antivirale active a présenté la plus forte affinité de liaison suivie de près par le dATP. En outre, le ténofovir a interagi dans la même poche que le remdesivir / dATP, mais a présenté une affinité de liaison et une stabilité de pose significativement plus faibles, ainsi qu'une liaison non fonctionnelle relativement stable avec le RdRp-CoV2 près de la poche active.
Discussion
Premièrement, nos résultats montrent que des concentrations intracellulaires similaires de remdesivir par rapport au dATP peuvent inhiber efficacement la réplication du SARS-CoV2. En effet, Gordon et al. ont rapporté une sélectivité élevée de l'antiviral sur l'incorporation de dATP en utilisant RdRp-CoV2 actif purifié. De plus, il a été rapporté que le remdesivir inhibe le SRAS-CoV-2 dans les cellules pulmonaires à des concentrations submicromolaires in vitro. De plus, un site de liaison similaire pour le remdesivir dans la polymérase du SARS-CoV-2 a été rapporté récemment par deux approches différentes, basées sur un alignement structurel en 3D utilisant d'autres polymérases virales [23] et une minimisation contrainte et recherche conformationnelle sur le RdRp-CoV2 site actif. En fait, notre modèle a fourni les interactions moléculaires spécifiques soutenant le site de liaison (voir le matériel supplémentaire S3 pour une description détaillée).contraignant .
En résumé, nos résultats sur l'interaction remdesivir-SRAS-CoV2 sont solidement alignés sur des études récentes et valide notre approche en tant que cadre fiable pour évaluer les analogues d'acides nucléiques contre le SRAS-CoV2. Nous concluons que l'efficacité clinique partielle observée pour le remdesivir n'est pas le résultat d'interactions moléculaires avec le RdRp-CoV2, étant donné sa forte affinité de liaison et la stabilité de la cible médicamenteuse. L'efficacité du remdesivir peut également reposer sur des propriétés pharmacocinétiques non étudiées et / ou sur le temps de traitement par rapport à la réplication virale.
En ce qui concerne le ténofovir, notre approche est la première à inclure l'ARN gabarit naissant dans l'ensemble et améliore encore les travaux antérieurs en utilisant des structures cryo-EM au lieu de l'homologie et par un échantillonnage plus étendu des poses de ligand à l'aide de calculs distribués par des volontaires. Conformément à nos résultats, il a été démontré que le ténofovir-diphosphate termine définitivement l'extension polymérase de l'ARN naissant lors de l'utilisation de RdRp-CoV2 recombinant. Cependant, la perfusion de ténofovir dans des cultures de cellules Vero n'a pas inhibé la réplication du SARS-CoV-2, tandis que l'utilisation de 3-90 μM de son promédicament TDF a entraîné une réduction de 15 fois de la libération du génome viral . De plus, l'utilisation de TDF / FTC pour traiter les furets infectés par le SRAS-CoV-2 a conduit à de meilleurs scores cliniques et à des titres viraux inférieurs dans les lavages nasaux par rapport à un placebo. A noter, la prodrogue TDF, formulé pour augmenter la biodisponibilité limitée du ténofovir, il est connu pour se diffuser passivement à travers les membranes cellulaires et s'activer davantage au niveau intracellulaire, contrairement au ténofovir qui nécessite un transport actif pour être ingéré avant l'activation. En effet, des niveaux plus élevés de métabolite actif après exposition au TDF par rapport au ténofovir ont été régulièrement rapportés dans plusieurs types de cellules. En revanche, le promédicament TAF a été formulé pour réduire les effets indésirables du médicament observés pour le TDF (qui se distribue dans tout le corps) en étant hautement spécifique des cellules cibles du VIH. Le TAF est bien connu pour activer sélectivement et présenter une distribution préférentielle dans les tissus lymphatiques. contrairement au ténofovir qui nécessite un transport actif pour être ingéré avant son activation [32,33]. En effet, des niveaux plus élevés de métabolite actif après exposition au TDF par rapport au ténofovir ont été régulièrement rapportés dans plusieurs types de cellules. En revanche, le promédicament TAF a été formulé pour réduire les effets indésirables du médicament observés pour le TDF (qui se répartit dans tout l'organisme) en étant hautement spécifique des cellules cibles du VIH. Le TAF est bien connu pour activer sélectivement et présenter une distribution préférentielle dans les tissus lymphatiques, par opposition au ténofovir qui nécessite un transport actif pour l'ingestion avant l'activation. En effet, des niveaux plus élevés de métabolite actif après exposition au TDF par rapport au ténofovir ont été régulièrement rapportés dans plusieurs types de cellules. En revanche, le promédicament TAF a été formulé pour réduire les effets indésirables du médicament observés pour le TDF (qui se répartit dans tout l'organisme) en étant hautement spécifique des cellules cibles du VIH. Le TAF est bien connu pour activer sélectivement et présenter une distribution préférentielle dans les tissus lymphatiques [37]. le promédicament TAF a été formulé pour réduire les événements indésirables observés pour le TDF (qui se distribue dans tout l'organisme) en étant hautement spécifique des cellules cibles du VIH. Le TAF est bien connu pour activer sélectivement et présenter une distribution préférentielle dans les tissus lymphatiques. Le promédicament TAF a été formulé pour réduire les événements indésirables observés pour le TDF (qui se distribue dans tout l'organisme) en étant hautement spécifique des cellules cibles du VIH. Le TAF est bien connu pour activer sélectivement et présenter une distribution préférentielle dans les tissus lymphatiques.
Nos résultats soutiennent une interaction sous-optimale ténofovir-RdRp-CoV2 par rapport au remdesivir, prédisant que l'ensemble est plus sensible à la concentration intracellulaire de la forme triphosphate. Ainsi, la mise en correspondance d'une disponibilité intracellulaire suffisante de ténofovir-diphostate avec le tropisme du SRAS-CoV2 (comme dans les voies respiratoires) est essentielle dans le confinement médicamenteux de la réplication virale, reflétant la prophylaxie du VIH. Il convient de noter que la réplication virale peut se produire dans différents tissus à différents stades cliniques. Ainsi, l'efficacité du ténofovir pourrait fortement dépendre du moment où il est administré par rapport à la distribution intra-hôte du SRAS-CoV-2. Avec les preuves pharmacocinétiques / pharmacodynamiques disponibles, nos résultats soutiennent que le TDF, parmi les composés à base de ténofovir, maximise l'efficacité à une posologie clinique sûre, en particulier lorsqu'elle est prise avant ou après l'exposition, en raison d'une perméation cellulaire élevée, d'une activation efficace des métabolites et d'une faible distribution sélective au niveau des tissus viraux ciblés, présentant une interprétation moléculaire plausible de l'incohérence apparente des composés à base de ténofovir contre le SRAS-CoV-2. Enfin, nos résultats soutiennent une évaluation plus poussée du remdesivir en tant que traitement contre COVID-19 mais aussi pour le promédicament TDF (disponible en tant que générique dans le monde entier), en particulier en tant que prophylaxie, tout en soulignant la nécessité de comprendre la disponibilité intracellulaire des médicaments dans Tissus ciblés par le SRAS-CoV2. présentant une interprétation moléculaire plausible de l’incohérence apparente des composés à base de ténofovir contre le SRAS-CoV-2. Enfin, nos résultats soutiennent une évaluation plus poussée du remdesivir en tant que traitement contre la COVID-19 mais aussi pour le promédicament TDF (disponible en tant que générique dans le monde entier), en particulier en tant que prophylaxie, tout en soulignant la nécessité de comprendre la disponibilité intracellulaire des médicaments dans les tissus ciblés par le SRAS-CoV2. présentant une interprétation moléculaire plausible de l’incohérence apparente des composés à base de ténofovir contre le SRAS-CoV-2. Enfin, nos résultats soutiennent une évaluation plus poussée du remdesivir en tant que traitement contre la COVID-19 mais aussi pour le promédicament TDF (disponible en tant que générique dans le monde entier), en particulier en tant que prophylaxie, tout en soulignant la nécessité de comprendre la disponibilité intracellulaire des médicaments dans Tissus ciblés par le SRAS-CoV2.
Méthodes
Structure du récepteur
La structure tridimensionnelle du RdRp-CoV2 résolue avec des chaînes d'ARN naissantes et matrices ainsi qu'avec deux ions magnésium sur le site de liaison a été obtenue à partir de la structure expérimentale déposée avec l'entrée 7BV1 de PDB (Protein Database Bank). Les cofacteurs Nsp7 et nsp8 ont été supprimés du modèle. Ici, le récepteur est marqué comme RdRp-CoV2-ARN.
Une approche d'amarrage d'ensemble est envisagée dans ce travail. Cette technique s'est avérée plus efficace qu'une expérience d'amarrage unique sur la structure cristalline. Par conséquent, les structures initiales du récepteur ont été soumises à des simulations de dynamique moléculaire sur plusieurs secondes, afin de se rapprocher de la flexibilité conformationnelle sur le récepteur. Les détails de la dynamique moléculaire (MD) sont donnés en tant que matériel supplémentaire, section S1.
Structure du ligand
Les structures tridimensionnelles du dATP et les formes biologiquement actives des médicaments remdesivir triphosphate et ténofovir diphosphate, ont été extraites de structures expérimentales contenant ces ligands dans le PDB. Avant les simulations d'amarrage, ces structures ont été préparées et soumises à une optimisation de la géométrie à l'aide de la fonction de corrélation d'échange Becke-Lee-Yang-Parr et du jeu de base triple numérique plus polarisation tel qu'implémenté dans le module Dmol3 de Materials Studio (Dassault Systemes BIOVIA, v20 .1.0). Dans tous les cas, la charge des molécules était de -4, correspondant aux groupements triphosphates totalement ionisés.
Amarrage moléculaire
Les structures de récepteur et de ligand ont été préparées en utilisant AutoDockTools v1.5.7 en supprimant les atomes isolés, en typant les atomes en types d'atomes AutoDock (AD4), en ajoutant des hydrogènes polaires, en éliminant les hydrogènes non polaires et en ajoutant des charges de Gasteiger. Le récepteur et les ligands ont été traités respectivement comme rigides et flexibles. Les liaisons rotatives des ligands ont été définies à l'aide des outils d'arbre de torsion dans AutoDockTools. Les structures des ligands, ainsi que le type d'atomes et les liaisons rotatives considérées dans les calculs d'amarrage, sont indiqués dans le matériel supplémentaire (Figure S1). Les expériences d'amarrage ont été réalisées avec AutoDock Vina 1.1.2, qui peut calculer les énergies de liaison avec un intervalle de précision de +/- 0,1 kcal / mol.
Pour fonctionner, AudoDock Vina nécessite de spécifier certains paramètres, tels que l'exhaustivité (le nombre de courses), la plage d'énergie et le nombre de modes de liaison. Après avoir effectué des calculs de test préliminaires pour établir les valeurs les plus appropriées, nous avons sélectionné les valeurs de paramètres suivantes : 20 analyses, 5 kcal / mol pour la plage d'énergie et 20 modes de liaison. Les structures utilisées dans l'amarrage sont disponibles auprès des auteurs sur demande.
Une recherche approfondie dans l'espace des conformations d'amarrage protéine-ligand a été soutenue par le projet d'informatique bénévole citoyen COVID-PHYM mis en œuvre à l'aide de la plate-forme BOINC (Berkeley Open Infrastructure for Network Computing). Environ 3,2 millions de poses ont été collectées pour chaque paire protéine (instantané) -ligand. Les détails concernant l'analyse des positions ancrées sont donnés en complément, section S2.
Pour la comparaison avec les approches précédentes, nous avons également effectué l'amarrage d'ensemble en utilisant le RdRp-CoV2 résolu sans ARN en utilisant la structure expérimentale déposée dans l'entrée PDB 7BTF [21] (matériel supplémentaire, section S3).
Disponibilité des données : Toutes les structures ligand-récepteurs sont disponibles auprès des auteurs sur demande.
Auteurs : Pablo M De Salazar, Javier Ramos, Victor L Cruz, Rosa Polo, Julia Del Amo, Javier Martínez-Salazar
Authorea. 28 septembre 2020
traduction :
- email : https://mailchi.mp/8e02e3ecd2cc/publicadopublished-preprint-del-proyecto-covid-phym?e=dccc8415b4
- article : https://www.authorea.com/users/362576/articles/483674-tenofovir-and-remdesivir-ensemble-docking-with-the-sars-cov-2-polymerase-and-template-nascent-rna


